phenylketonuria
มันคืออะไร ?
ฟีนิลคีโตนูเรียเป็นโรคที่มีลักษณะไม่ดูดซึม (หรือไม่เผาผลาญ) ของฟีนิลอะลานีน
ฟีนิลอะลานีนเป็นกรดอะมิโนจำเป็นที่มีบทบาทพื้นฐานในระบบประสาทโดยการกระตุ้นต่อมไทรอยด์ นอกจากนี้ยังเป็นสารกระตุ้นทางปัญญาอีกด้วย กรดอะมิโนนี้ไม่ได้ถูกสังเคราะห์โดยร่างกาย ดังนั้นจึงต้องจัดหาให้ by อาหาร. ที่จริงแล้ว ฟีนิลอะลานีนเป็นหนึ่งในองค์ประกอบของอาหารทั้งหมดที่อุดมไปด้วยโปรตีนจากสัตว์และพืช เช่น เนื้อสัตว์ ปลา ไข่ ถั่วเหลือง นม ชีส ฯลฯ
เป็นโรคทางพันธุกรรมและกรรมพันธุ์ที่พบได้ยาก ซึ่งส่งผลกระทบต่อทั้งเด็กหญิงและเด็กชาย โดยไม่ได้ให้ความสำคัญเป็นพิเศษ
หากตรวจไม่พบโรคตั้งแต่เนิ่นๆ เพื่อรักษาอย่างรวดเร็ว อาจเกิดการสะสมของสารนี้ในร่างกายและโดยเฉพาะอย่างยิ่งในระบบประสาท ฟีนิลอะลานีนในสมองที่กำลังพัฒนามากเกินไปนั้นเป็นพิษ
ฟีนิลอะลานีนส่วนเกินที่มีอยู่ในร่างกายจะถูกขับออกจากระบบไต ดังนั้นจึงพบในปัสสาวะของผู้ป่วยในรูปของฟีนิลคีโตน (2)
ในฝรั่งเศส การตรวจคัดกรองฟีนิลอะลานีนเป็นระบบตั้งแต่แรกเกิด: การทดสอบ Guthrie
ความชุก (จำนวนผู้ที่เป็นโรคในประชากรในช่วงเวลาหนึ่ง) ขึ้นอยู่กับประเทศที่เกี่ยวข้องและสามารถเปลี่ยนแปลงได้ระหว่าง 1 / 25 ถึง 000 / 1
ในฝรั่งเศส ความชุกของฟีนิลคีโตนูเรียคือ 1 / 17 (000)
โรคนี้รักษาด้วยการรับประทานอาหารที่มีโปรตีนต่ำ เพื่อลดระดับฟีนิลอะลานีนในร่างกายของผู้ป่วยและจำกัดความเสียหายของสมอง
การรักษาโรคในระยะเริ่มต้นมักจะป้องกันการพัฒนาของอาการ
นอกจากนี้ การรักษาที่ล่าช้าซึ่งนำไปสู่การสะสมของโมเลกุลนี้ในสมองก็มีผลที่ตามมาโดยเฉพาะ: (3)
– ปัญหาการเรียนรู้;
– ความผิดปกติทางพฤติกรรม;
– โรคลมบ้าหมู;
– กลาก
มีการแสดงโรคสามรูปแบบหลังการตรวจเลือดเมื่อแรกเกิด: (2)
– ฟีนิลคีโตนูเรียทั่วไป: มีฟีนิลอะลานีเมีย (ระดับฟีนิลอะลานีนในเลือด) มากกว่า 20 มก. / ดล. (หรือ 1 ไมโครโมล / ลิตร);
– ฟีนิลคีโตนูเรียผิดปกติ: มีระดับระหว่าง 10 ถึง 20 มก. / ดล. (หรือ 600-1 µmol / l);
– hyperphenylalaninemia ปานกลาง (HMP) ถาวร โดยที่ phenylalaninemia มีค่าน้อยกว่า 10 mg / dl (หรือ 600 μmol / l) รูปแบบของโรคนี้ไม่ร้ายแรงและต้องการการตรวจสอบอย่างง่ายเพื่อหลีกเลี่ยงการทำให้รุนแรงขึ้น
อาการ
การตรวจคัดกรองอย่างเป็นระบบตั้งแต่แรกเกิดทำให้ในกรณีส่วนใหญ่สามารถจำกัดลักษณะอาการทั่วไปของโรคได้
การรักษาโรคนี้ขึ้นอยู่กับอาหารที่มีโปรตีนต่ำ และการเฝ้าติดตามฟีนิลอะลานีนีเมียยังช่วยป้องกันการสะสมของฟีนิลอะลานีนในร่างกายและโดยเฉพาะอย่างยิ่งในสมอง (2)
ในกรณีที่ไม่ได้ทำการวินิจฉัยทารกแรกเกิด อาการของฟีนิลคีโตนูเรียจะปรากฏขึ้นอย่างรวดเร็วหลังคลอดและอาจรุนแรงมากหรือน้อยขึ้นอยู่กับรูปแบบของโรค
อาการเหล่านี้มีลักษณะดังนี้:
- ความล่าช้าในการพัฒนาจิตใจของเด็ก
– การเจริญเติบโตช้า
– microcephaly (ขนาดกะโหลกศีรษะเล็กผิดปกติ);
– อาการชักและแรงสั่นสะเทือน;
– กลาก;
– อาเจียน ;
– ความผิดปกติทางพฤติกรรม (สมาธิสั้น);
- ความผิดปกติของมอเตอร์
ในกรณีของ hyperphenylalaninemia การกลายพันธุ์ในยีนที่เข้ารหัสปัจจัยร่วมในการเปลี่ยนฟีนิลอะลานีนเป็นไทโรซีน (co-factor BHA) เป็นไปได้ การรบกวนเหล่านี้ในการผลิตไทโรซีนนำไปสู่:
– ผิวขาว;
- ผมสวย
ที่มาของโรค
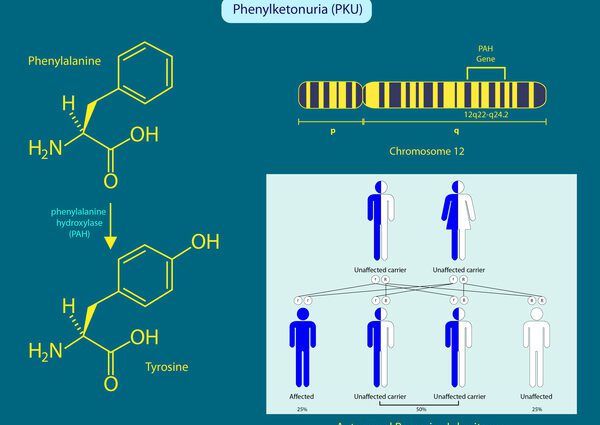
ฟีนิลอะลานีนเป็นโรคทางพันธุกรรมที่สืบทอดมา ส่งผลให้เกิดการถ่ายทอดทางพันธุกรรมแบบถอยอัตโนมัติ โหมดการส่งสัญญาณนี้เกี่ยวข้องกับออโตโซม (โครโมโซมที่ไม่ใช่ทางเพศ) และภาวะถดถอยส่งผลให้ต้องให้ผู้รับการทดลองมีอัลลีลที่กลายพันธุ์สองชุดเพื่อพัฒนาฟีโนไทป์ที่เป็นโรค (4)
ที่มาของโรคคือการกลายพันธุ์ของยีน PAH (12q22-q24.2) รหัสยีนนี้เป็นรหัสของเอนไซม์ที่ยอมให้ไฮโดรไลซิส (ทำลายสารด้วยน้ำ): ฟีนิลอะลานีนไฮดรอกซีเลส
ยีนที่กลายพันธุ์จึงส่งผลให้การทำงานของฟีนิลอะลานีนไฮดรอกซีเลสลดลง ดังนั้นจึงไม่สามารถแปรรูปฟีนิลอะลานีนจากอาหารได้อย่างมีประสิทธิภาพโดยร่างกาย ระดับของกรดอะมิโนนี้ในเลือดของผู้ที่ได้รับผลกระทบจึงเพิ่มขึ้น หลังจากการเพิ่มขึ้นของปริมาณฟีนิลอะลานีนในร่างกาย การจัดเก็บจะเกิดขึ้นในอวัยวะและ/หรือเนื้อเยื่อต่างๆ โดยเฉพาะในสมอง (4)
มีการแสดงให้เห็นการกลายพันธุ์อื่นๆ ในความสัมพันธ์กับโรคนี้ สิ่งเหล่านี้เป็นการดัดแปลงที่ระดับของยีนที่เข้ารหัส BHA (ปัจจัยร่วมสำหรับการเปลี่ยนฟีนิลอะลานีนเป็นไทโรซีน) และโดยเฉพาะอย่างยิ่งเกี่ยวข้องกับรูปแบบของไฮเปอร์ฟีนิลอะลานีเมีย (1)
ปัจจัยเสี่ยง
ปัจจัยเสี่ยงที่เกี่ยวข้องกับโรคคือพันธุกรรม อันที่จริงการแพร่กระจายของโรคนี้เกิดขึ้นจากการถ่ายโอน autosomal recessive ต้องมีการปรากฏตัวของอัลลีลทั้งสองที่กลายพันธุ์สำหรับยีนในแต่ละคนเพื่อพัฒนาโรค
ในแง่นี้ ผู้ปกครองแต่ละคนของผู้ป่วยจะต้องมีสำเนาของยีนกลายพันธุ์ เนื่องจากเป็นรูปแบบด้อย ผู้ปกครองที่มียีนกลายพันธุ์เพียงสำเนาเดียวจึงไม่แสดงอาการของโรค อย่างไรก็ตาม จำเป็นต้องมีมากถึง 50% ในแต่ละยีนที่ถ่ายทอดยีนกลายพันธุ์ไปยังลูกหลาน หากบิดาและมารดาของเด็กแต่ละคนถ่ายทอดยีนกลายพันธุ์ ผู้รับการทดลองจะมีอัลลีลที่กลายพันธุ์ทั้งสองอัลลีล และจากนั้นจะพัฒนาฟีโนไทป์ที่เป็นโรค (4)
การป้องกันและรักษา
การวินิจฉัย phenylketonuria ส่วนใหญ่ทำผ่านโปรแกรมคัดกรองการเกิด: การตรวจคัดกรองทารกแรกเกิดอย่างเป็นระบบ นี่คือการทดสอบกูทรี
การทดสอบนี้ถือเป็นผลบวกหากระดับฟีนิลอะลานีนในเลือดมากกว่า 3 มก. / ดล. (หรือ 180 ไมโครโมล / ลิตร) ในบริบทของภาวะฟีนิลอะลานีเมียที่มากเกินไป การตรวจเลือดครั้งที่สองจะดำเนินการในศูนย์เฉพาะทางเพื่อยืนยันว่ามีฟีนิลคีโตนูเรียหรือไม่ หากระดับฟีนิลอะลานีนยังคงมากกว่า 3 มก. / ดล. ในระหว่างการให้ยาครั้งที่สองและไม่ได้ระบุโรคที่อาจมีความรับผิดชอบอื่น ๆ การวินิจฉัยจะทำขึ้น (2)
การวินิจฉัยโรคนี้ควรแยกออกจากการขาด BH4 อันที่จริงลักษณะหลังนี้เป็นลักษณะเฉพาะของภาวะ hyperphenylalaninemia และต้องการการตรวจสอบอย่างง่ายเท่านั้น ในขณะที่การตรวจหาฟีนิลคีโตนูเรียในตัวอย่างต้องได้รับการดูแลเป็นพิเศษและอาหารที่มีโปรตีนต่ำ (1)
การรักษาเบื้องต้นสำหรับฟีนิลคีโตนูเรียจึงเป็นอาหารที่มีฟีนิลอะลานีนต่ำ กล่าวคือ การบริโภคโปรตีนในอาหารลดลง อาหารโปรตีนต่ำนี้จะต้องดำเนินการทันทีที่มีการตรวจคัดกรองทารกแรกเกิด ต้องติดตามตลอดชีวิตและอาจเข้มงวดมากหรือน้อยขึ้นอยู่กับเรื่องและรูปแบบของโรค (2)
นอกจากอาหารที่มีฟีนิลอะลานีนในอาหารนี้แล้ว ผู้ป่วยยังสามารถกำหนดซาโพรเทริน ไดไฮโดรคลอไรด์ให้กับผู้ป่วยได้ เพื่อให้อาหารของเขาเข้มงวดน้อยลง หรือแม้กระทั่งให้อาหารของเขายังคงปกติ (2)
นอกจากนี้ อาจมีการแนะนำผลิตภัณฑ์เสริมอาหารที่อุดมไปด้วยกรดอะมิโน (ยกเว้นฟีนิลอะลานีน) วิตามินและแร่ธาตุเพื่อฟื้นฟูความไม่สมดุลในการบริโภคเหล่านี้เนื่องจากอาหารนี้ (3)
ควรหลีกเลี่ยงการบริโภคแอสพาเทม (สารให้ความหวานเทียมที่ใช้ในผลิตภัณฑ์หลายประเภท เช่น เครื่องดื่มในอุตสาหกรรม การเตรียมอาหาร ฯลฯ) สำหรับผู้ที่เป็นโรคฟีนิลคีโตนูเรีย ในความเป็นจริง เมื่อดูดซึม แอสพาเทมจะเปลี่ยนในร่างกายเป็นฟีนิลอะลานีน ในแง่นี้ เพิ่มความเสี่ยงของการสะสมของโมเลกุลนี้ในร่างกายและความเสี่ยงที่จะเป็นพิษต่อผู้ป่วย แอสพาเทมมีอยู่ในยาหลายชนิดต้องให้ความสนใจเป็นพิเศษจากผู้ป่วยเมื่อทานยาบางชนิด
ในแง่ของการป้องกัน เนื่องจากการแพร่กระจายของโรคเป็นกรรมพันธุ์ ครอบครัวที่ได้รับผลกระทบจากโรคสามารถขอความช่วยเหลือและคำแนะนำทางพันธุกรรมได้
การพยากรณ์โรคจะแปรผันขึ้นอยู่กับผู้ป่วยและรูปแบบของโรค